Когнитивный резерв: Что такое когнитивный резерв и как он работает — Сноб
Когнитивный резерв, когнитивные нарушения и возможность их медикаментозной коррекции
Одной из наиболее серьезных медико-социальных проблем на сегодняшний день является проблема деменции. Это связано с целым рядом причин, в частности с ростом продолжительности жизни, увеличением в популяции доли лиц пожилого и старческого возраста, изменением особенностей образа жизни, включая характер и объем физических и эмоциональных нагрузок, рациона питания, воздействия целого ряда химических факторов, повышением качества диагностики и совершенствованием методов выявления когнитивных нарушений. Исключительная важность проблемы обусловлена и большими материальными расходами, которые связаны не только с лечением пациента с деменцией, но и с осуществлением мероприятий по обеспечению его жизнедеятельности, ухода за ним.
Материальные затраты на пациентов с деменцией исключительно высоки и демонстрируют неуклонную тенденцию к дальнейшему нарастанию. Так, в США в последнюю декаду ХХ века они возросли втрое и вдвое они могут возрасти к 2030 г.
Наблюдается зависимость нарастания частоты деменции с возрастом. Так, деменция выявляется у 5% лиц старше 65 лет, тогда как среди лиц старше 85 лет она выявляется уже у 50% населения [5]. В Российской Федерации при относительно невысокой средней продолжительности жизни доля пожилых в обществе также неуклонно увеличивается [6].
Важнейшими причинами развития деменции являются болезнь Альцгеймера (БА), сосудистые поражения головного мозга, нейродегенеративные заболевания (болезнь Паркинсона, деменция с тельцами Леви, болезнь Гентингтона и др.
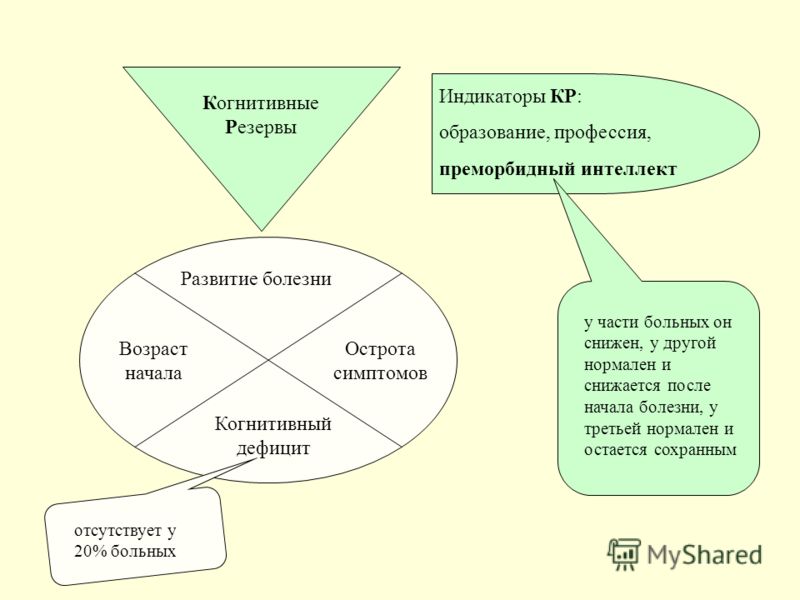
В качестве одного из факторов, потенциально способных замедлить наступление деменции и сделать ее течение более мягким, большой практический и теоретический интерес представляет концепция когнитивного резерва (КР) [7, 8]. В соответствии с данной концепцией, вероятность развития деменции определяют врожденные структурно-функциональные особенности головного мозга, а также такие приобретенные факторы, как уровень образования и интеллектуальных нагрузок в течение жизни, характер трудовой деятельности и стиль проведения досуга. Ранее предполагалось, что наиболее значимым для последующего развития интеллекта индивидуума является полученный в раннем детстве опыт [9], однако последующие исследования показали, что важный вклад в формирование КР вносит поддержание интеллектуальной деятельности в течение последующей жизни [10]. Более высокий уровень испытываемых индивидуумом в течение жизни интеллектуальных нагрузок и высокий уровень образования связаны с меньшей вероятностью развития когнитивных расстройств в последующем.
На состояние КР оказывают влияние образ социального поведения, положение индивидуума в социальной иерархии, хотя результаты таких исследований носят неоднозначный характер. Так, изначально более высокий уровень интеллектуального развития и более активное социальное поведение, связанное с трудовой деятельность и проведением досуга, способствуют большей сохранности когнитивных функций в пожилом возрасте [11]. Некоторые исследователи [12] считают, что более высокий исходный уровень КР, особенности образа жизни и социально-экономическое положение способны оказывать превентивное действие в отношении развития БА и возрастного когнитивного снижения. Одним из факторов, обеспечивающих формирование и поддержание высокого уровня КР, является также билингвизм [13], делающий возможным переключение с одного языка на другой в процессе общения и построении грамматически правильных фраз, что требует высокоэффективных процессов контроля. Сказанное подтверждается наблюдениями, что многие нейропсихологические тесты намного лучше выполняются владеющими двумя языками взрослыми и пожилыми лицами, чем их ровесниками, владеющими только одним языком.
Однако предшествующий развитию заболевания КР не всегда в полной мере способен оказать свое протективное действие. Так, A. Singh-Manoux и соавт. [14] при наблюдении за 8000 государственных служащих Лондона (средний возраст 56±6 лет), установили, что уровень КР коррелировал с исходным уровнем когнитивных функций, при этом наиболее сильная корреляционная связь имелась с занимаемой должностью. Вместе с тем выраженность когнитивного снижения к окончанию периода наблюдения оказалась максимальной у лиц, занимавших наиболее высокие административные должности. Метаанализ значительного числа клинических исследований (в них было включено более 29 000 обследованных) показал, что высокий исходный уровень КР ассоциирован с 50% снижения риска развития деменции в последующем [15].
Подтверждение защитной роли КР в отношении развития деменции было получено N. Scarmeas и соавт. [10] при изучении состояния мозгового кровотока методом позитронно-эмиссионной томографии (ПЭТ) у пациентов с БА (снижение мозгового кровотока является косвенным маркером, подтверждающим выраженность структурных изменений вещества головного мозга при нейродегенеративном процессе [16]).
Можно выделить активный и пассивный механизмы формирования КР. Пассивный включает такие структурные характеристики мозга, как его объем, количество функционирующих синапсов, обладающих буферными функциями по отношению к повреждению [18].
Одним из механизмов защитных эффектов КР в условиях старения является реорганизация некоторых церебральных структур, ответственных за выполнение тех или иных функций, в частности речевых [19]. В зависимости от выполняемых задач наблюдается перераспределение активности между полушариями, а также между передними и задними отделами головного мозга. Благодаря этому обеспечивается оптимизация выполнения когнитивных функций, что делает возможным эффективное выполнение различных видов деятельности даже в условиях структурного поражения мозгового вещества вследствие старения.
Имеются морфологические подтверждения роли КР в предупреждении когнитивных нарушений. Так, при исследовании аутопсийного мозга пациентов, у которых при жизни отсутствовали когнитивные нарушения, в ряде случаев выявлялись различной степени выраженности изменения, характерные для БА [20]. Интересны прижизненные исследования C. Wiley и соавт. [21], проведенные на основании оценки интенсивности накопления в ткани головного мозга специфического маркера, позволяющего визуализировать амилоидные накопления при БА. Речь идет о питтсбургском соединении В (Pittsburgh compound B), выявляемом при помощи ПЭТ. Было установлено, что его максимальное накопление отмечается на развернутых стадиях БА, при этом его количество коррелирует с грубым когнитивным дефицитом. Однако D. Rentz и соавт. [22] показали, что такая зависимость характерна для пациентов с относительно низким КР, при более высоком его уровне, несмотря на обильные отложения амилоида, когнитивные функции остаются более сохранными.
Практическая значимость концепции КР состоит в том, что его использование позволяет планировать стратегии индивидуальной профилактики развития деменции с использованием различных лекарственных и немедикаментозных воздействий. В ряде клинических исследований [23, 24], посвященных изучению данной проблемы, было показано, что когнитивные тренировки различной модальности способны не только замедлить развитие когнитивного снижения у пожилых людей, но и улучшить их мыслительные способности. Как свидетельствуют результаты одного из масштабных пятилетних исследований [25], в которое были включены 2800 пациентов, проходивших систематический тренинг, направленный на улучшение когнитивных функций, положительный эффект сохранялся на протяжении всего периода исследования.
В ряде клинических исследований [23, 24], посвященных изучению данной проблемы, было показано, что когнитивные тренировки различной модальности способны не только замедлить развитие когнитивного снижения у пожилых людей, но и улучшить их мыслительные способности. Как свидетельствуют результаты одного из масштабных пятилетних исследований [25], в которое были включены 2800 пациентов, проходивших систематический тренинг, направленный на улучшение когнитивных функций, положительный эффект сохранялся на протяжении всего периода исследования.
Роль КР в предупреждении развития тяжелой деменции и замедления темпов когнитивного снижения не исключает применения адекватно подобранной медикаментозной терапии. Ее выбор определяется представлениями о патогенетических механизмах развития деменции.
В настоящее время достаточно подробно изучены молекулярные и клеточные механизмы развития деменции как при нейродегенеративных заболеваниях, в частности, при БА, так и при сосудистом поражении головного мозга.

Избыточная активность глутамат- и аспартатергической нейротрансмиссии связана с целым рядом негативных эффектов. Считается, что чрезмерная, в том числе длительная активация соответствующих рецепторов, ведет к избыточному возбуждению постсинаптических нейронов, неадекватному притоку ионов кальция в нервные клетки по рецептор-ассоциированным ионным каналам и ряду других негативных последствий [28]. Итогом этих процессов является повреждение и гибель нейронов, что было убедительно продемонстрировано на моделях повреждения головного мозга (острая ишемия, травма, нейродегенерация и др.), а также в клинических условиях [29]. Показана возможность отсроченной гибели нейронов, в частности, по механизму апоптоза, вследствие эксайтотоксичности, а также потенциально обратимое нарушение их функции, которое может рассматриваться в качестве объекта терапевтического вмешательства.
Предпринимались попытки фармакологической регуляции глутаматергической нейротрансмиссии, ряд из которых окончился неудачно из-за того, что значительное ее угнетение приводило к расстройствам сознания, поведения, нарастанию когнитивных нарушений [30, 31]. Вследствие этого некоторые лекарственные препараты, оказывавшие определенный эффект в условиях эксперимента, не получили применения в клинической практике.
Вследствие этого некоторые лекарственные препараты, оказывавшие определенный эффект в условиях эксперимента, не получили применения в клинической практике.
В связи со сказанным значительный интерес представляет мемантин, новой торговой маркой которого является препарат меманталь. В результате проведенных фармакологических исследований была подтверждена полная биоэквивалентность меманталя оригинальному препарату.
Мемантин (меманталь) является умеренно аффинным неконкурентным антагонистом потенциалзависимых НМДА-рецепторов. Исключительно важной его особенностью является то, что он способен предохранять нейроны от повреждения в условиях избыточного выброса глутамата в синаптическую щель [32, 33]. В то же время, принципиальным отличием от многих изучавшихся антагонистов глутаматных рецепторов, особенность мемантина заключается в том, что при его назначении отсутствует угнетение нейротрансмиссии в нормально функционирующих синапсах, вследствие чего применение в терапевтических дозировках не сопровождается расстройствами сознания и когнитивными нарушениями.
В экспериментальных исследованиях была установлена эффективность мемантина как в культурах нервной ткани, так и в моделях дегенеративного поражения мозгового вещества у животных.
Очередным этапом изучения препарата явилось проведение рандомизированных клинических исследований в тщательно отобранных группах пациентов. Одним из них является исследование I. Aprahamian и соавт. [34], касавшиеся пациентов с БА. Полученные в таких работах результаты были неоднократно проанализированы, о чем свидетельствуют ряд опубликованных метаанализов и систематизированных обзоров.
Серьезной проблемой в терапии заболеваний, приводящих к деменции, является возможность ее раннего распознавания. Было показано [35], что выявление пациентов на преддементной стадии способно обеспечить своевременное начало лечения и соответственно относительно более благоприятный исход заболевания. Вместе с тем вопрос о том, насколько эффективны такие мероприятия в масштабах популяции, в частности как велика значимость скрининга и других способов раннего выявления когнитивных нарушений и насколько они способны предотвратить развитие деменции, остается открытым [36].
Опубликованы результаты многочисленных рандомизированных клинических исследований [37-39], в которых были получены достаточно убедительные данные в отношении высокой эффективности мемантина при деменции у пациентов с БА. Накоплен отечественный опыт применения мемантина при БА смешанной деменции и деменции с тельцами Леви [40]. Установлено, что наиболее выраженным и стойким эффект оказался у больных с АД и смешанной деменцией. Положительный эффект заключался преимущественно в уменьшении выраженности модально-неспецифических нарушений памяти, улучшении способности к обобщению, выстраиванию программы действия и контролю за выполняемыми операциями; было отмечено замедление когнитивного снижения в процессе терапии. Более стабильный эффект наблюдался при длительном приеме препарата.
Предпринимались попытки оценки эффективности применения мемантина в зависимости от выраженности когнитивных нарушений на момент начала терапии. Так, проведенный в Швеции метаанализ [41] был основан на результатах 6 рандомизированных исследований, в которые были включены 1826 пациентов с умеренно выраженной и тяжелой деменцией (по MMSE не более 20 баллов) при БА. Был сделать вывод о том, что применение мемантина при достаточно длительном сроке обеспечивает не только улучшение мнестических функций и способности к обучению, повышение эффективности выполнения ряда психометрических тестов, но и расширение способности к самообслуживанию и повышению качества жизни больных [49].
Был сделать вывод о том, что применение мемантина при достаточно длительном сроке обеспечивает не только улучшение мнестических функций и способности к обучению, повышение эффективности выполнения ряда психометрических тестов, но и расширение способности к самообслуживанию и повышению качества жизни больных [49].
Проводилось также изучение эффективности мемантина у пациентов с менее выраженными когнитивными нарушениями вследствие БА (по MMSE от 20 до 23 баллов). В одном из предварительных рандомизированнных исследований [42] были получены достаточно обнадеживающие результаты, в частности, при лечении больных, получавших мемантин на протяжении 24 нед. Но менее убедительными оказались результаты проведенного в последующем метаанализа [43]: не было установлено положительного эффекта проводимой терапии в виде улучшения когнитивных функций или замедления их снижения. Тем не менее результаты приведенных выше и других рандомизированных контролируемых исследований явились основанием для рекомендаций в отношении применения мемантина пациентам с умеренно выраженной и тяжелой деменцией при БА в странах Европейского Союза (2002) и США (2003) [43].
Целый ряд последующих исследований был посвящен анализу эффективности мемантина у пациентов не только с БА, но и другими формами деменции. Результаты рандомизированных исследований, посвященных оценке лечения пациентов с различными типами деменции (БА, сосудистая деменция, деменция смешанного типа и др.), были повторно проанализированы в систематизированных обзорах [43]. Их авторы отметили, что применение мемантина эффективно у пациентов с различными типами деменции, более выраженный эффект наблюдается при использовании высоких доз препарата (20 мг в сутки) на протяжении достаточного периода времени (6 нед и более). Отмечена хорошая переносимость препарата даже при длительном лечении. Из побочных эффектов зарегистрированы эпизоды психомоторного возбуждения у отдельных пациентов [45].
Активно изучалась возможность назначения мемантина у больных с деменцией с тельцами Леви [46], что нашло отражение в метаанализе таких исследований, которые позволили установить, что при этом заболевании проведенное лечение оказалось менее эффективным, чем у пациентов с БА, хотя по ряду оцениваемых параметров мемантин был эффективнее плацебо. Кроме того, авторы констатировали хорошую переносимость терапии и незначительное число побочных явлений.
Кроме того, авторы констатировали хорошую переносимость терапии и незначительное число побочных явлений.
Сопоставимые результаты были получены и в ходе другого исследования [47], в котором пациенты с легкой и умеренной деменцией вследствие болезни Паркинсона и деменции с тельцами Леви получали мемантин по 20 мг в сутки на протяжении 24 нед. Авторы отметили улучшение в соответствии с оценкой состояния по шкале CGI, тогда как по другим шкалам существенного улучшения зарегистрировано не было. Было высказано предположение [48], что положительный эффект препарата при смешанных деменциях может быть обусловлен угнетением специфических для БА патогенетических механизмов развития заболевания. Интерес представляет тот факт, что мемантин не только обеспечивает стабилизацию или улучшение состояния когнитивных функций у больных болезнью Паркинсона и деменцией с тельцами Леви, но и обеспечивает повышение качества их жизни и расширение способности к самообслуживанию [49].
Таким образом, полученные к настоящему времени результаты применения мемантина свидетельствую о том, что его он оказывает положительный эффект при разных типах деменции, что позволяет рассматривать его как противодементный препарат с достаточно широким спектром действия, применение которого целесообразно и у пациентов с неустановленной и смешанной этиологией, в частности при сочетании БА с деменциями другого генеза [32]. Перспективным в этом отношении представляется применение препарата меманталь, эффективность которого продемонстрирована и доказана в ряде клинических исследований.
Перспективным в этом отношении представляется применение препарата меманталь, эффективность которого продемонстрирована и доказана в ряде клинических исследований.
сравнительный анализ жителей Санкт-Петербурга и Нижнего Новгорода
2018 №6 — перейти к содержанию номера…
Постоянный адрес этой страницы — https://mir-nauki.com/133psmn618.html
Полный текст статьи в формате PDF (объем файла: 353.5 Кбайт)
Ссылка для цитирования этой статьи:
Стрижицкая, О. Ю. Когнитивный резерв и психологическое благополучие: сравнительный анализ жителей Санкт-Петербурга и Нижнего Новгорода / О. Ю. Стрижицкая, Т. С. Харитонова // Интернет-журнал «Мир науки». — 2018 №6. — URL: https://mir-nauki.com/PDF/133PSMN618.pdf (дата обращения: 16.03.2023).
Когнитивный резерв и психологическое благополучие: сравнительный анализ жителей Санкт-Петербурга и Нижнего Новгорода
Стрижицкая Ольга Юрьевна
ФГБОУ ВО «Санкт-Петербургский государственный университет», Санкт-Петербург, Россия
Доктор психологических наук, доцент
E-mail: o. [email protected]
[email protected]
ORCID: http://orcid.org/0000-0002-7141-162X
РИНЦ: https://elibrary.ru/author_profile.asp?id=552909
SCOPUS: http://www.scopus.com/authid/detail.url?authorId=56766238600
Харитонова Татьяна Сергеевна
ФГБОУ ВО «Санкт-Петербургский государственный экономический университет», Санкт-Петербург, Россия
Старший преподаватель
E-mail: [email protected]
ORCID: http://orcid.org/0000-0002-9019-4982
РИНЦ: https://elibrary.ru/author_profile.asp?id=958547
Аннотация. Статья посвящена сравнительному анализу особенностей когнитивного резерва и его соотношения с психологическим благополучием в пожилом возрасте в Санкт-Петербурге и Нижнем Новгороде. Когнитивный резерв – это достаточно новый, но при этом перспективный механизм, который позволяет снизить проявления когнитивных дегенеративных процессов в период старения. Когнитивный резерв основан на когнитивно-стимулирующих видах деятельности, которые человек осуществляет в течение жизни, и потому может быть чувствителен не только к культурным различиям между странами, но и внутри таких неоднородных по составу стран как, например, Россия. Целью исследования было сравнить особенности функционирования когнитивного резерва пожилых людей в Санкт-Петербурге и Нижнем Новгороде.
Целью исследования было сравнить особенности функционирования когнитивного резерва пожилых людей в Санкт-Петербурге и Нижнем Новгороде.
В исследовании приняли участие 200 респондентов в возрасте 50-81 лет из Санкт-Петербурга (N = 100, Мвозраст = 68,39) и Нижнего Новгорода (N = 100, Мвозраст = 67,88). В качестве методов использовались Индекс когнитивного резерва, Шкала психологического благополучия.
Результаты исследования показали, что уровневые показатели когнитивного резерва у респондентов из обоих городов сходны, при этом наблюдаются различия в структурных связях между ними. Респонденты из Санкт-Петербурга демонстрируют меньше внутрифункциональных связей показателей когнитивного резерва, при этом демонстрируя прямую связь с показателями психологического благополучия. Нижегородцы демонстрируют картину связей, согласующуюся с результатами западных исследований в большей степени, но при этом не обнаруживают прямых связей с психологическим благополучием. Таким образом, полученные данные подтверждают идею о том, что социально-демографические и культурно-исторические условия могут влиять на функционирование когнитивного резерва.
Ключевые слова: когнитивный резерв; психологическое благополучие; позитивное старение; старение; поздняя взрослость; образование; профессиональная деятельность; досуговая деятельность
Скачать
Уважаемые читатели! Комментарии к статьям принимаются на русском и английском языках.
Комментарии проходят премодерацию, и появляются на сайте после проверки редактором.
Комментарии, не имеющие отношения к тематике статьи, не публикуются.
Когнитивный резерв при старении и болезни Альцгеймера
1. Гурланд Б. Границы деменции: влияние социокультурных характеристик на частоту деменции, возникающей в старческом возрасте. Старение. 1981; 15: 61–84. [Google Scholar]
2. Kittner SJ, White LR, Farmer ME, Wolz M, Kaplan E, Moes E, et al. Методологические вопросы скрининга деменции: проблема адаптации образования. Журнал хронических болезней. 1986; 39: 163–170. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
3. Беркман Л.Ф. Связь между уровнем образования и обследованиями психического статуса: имеет этиологическое значение для старческого слабоумия или нет? Журнал хронических болезней. 1986;39:171–174. [PubMed] [Google Scholar]
4. Zhang M, Katzman R, Salmon D, Jin H, Cai G, Wang Z, et al. Распространенность деменции и болезни Альцгеймера в Шанхае, Китай: влияние возраста, пола и образования. Анналы неврологии. 1990; 27: 428–437. [PubMed] [Google Scholar]
5. Elkins JS, Longstreth WT, Manolio TA, Newman AB, Bhadelia RA, Johnston SC. Образование и снижение когнитивных функций, связанные с инфарктом головного мозга, определенным с помощью МРТ. Неврология. 2006;67(3):435–440. [PubMed] [Академия Google]
6. Dufouil C, Alperovitch A, Tzourio C. Влияние образования на взаимосвязь между поражениями белого вещества и познанием. Неврология. 2003;60(5):831–836. [PubMed] [Google Scholar]
7. Dufouil C, Alperovitch A, Ducros V, Tzourio C. Гомоцистеин, гиперинтенсивность белого вещества и когнитивные функции у здоровых пожилых людей. Энн Нейрол. 2003;53(2):214–221. [PubMed] [Google Scholar]
Гомоцистеин, гиперинтенсивность белого вещества и когнитивные функции у здоровых пожилых людей. Энн Нейрол. 2003;53(2):214–221. [PubMed] [Google Scholar]
8. Glatt SL, Hubble JP, Lyons K, Paolo A, Troster AI, Hassanein RE, et al. Факторы риска деменции при болезни Паркинсона: влияние образования. Нейроэпидемиология. 1996;15:20–25. [PubMed] [Google Scholar]
9. Kesler SR, Adams HF, Blasey CM, Bigler ED, et al. Преморбидное интеллектуальное функционирование, образование и размер мозга при черепно-мозговой травме: исследование гипотезы когнитивного резерва. Прикладная нейропсихология. 2003; 10: 153–162. [PubMed] [Google Scholar]
10. Farinpour R, Miller EN, Satz P, Selnes OA, Cohen BA, Becker JT, et al. Психосоциальные факторы риска заболеваемости и смертности от ВИЧ: результаты многоцентрового когортного исследования СПИДа (MACS), журнал клинической и экспериментальной нейропсихологии. 2003; 25: 654–670. [PubMed] [Академия Google]
11. Барнетт Дж.Х., Салмонд К. Х., Джонс П.Б., Саакян Б.Дж. Когнитивный резерв в нейропсихиатрии. Психологическая медицина. 2006; 36: 1053–1064. [PubMed] [Google Scholar]
Х., Джонс П.Б., Саакян Б.Дж. Когнитивный резерв в нейропсихиатрии. Психологическая медицина. 2006; 36: 1053–1064. [PubMed] [Google Scholar]
12. Sumowski JF, Chiaravalloti N, Deluca J. Когнитивный резерв защищает от когнитивной дисфункции при рассеянном склерозе. J Clin Exp Neuropsychol. 2009;31(8):913–926. [PubMed] [Google Scholar]
13. Katzman R, Robert T, DeTeresa R, Brown T, Peter D, Fuld P, et al. Клинико-патологические и нейрохимические изменения при деменции: подгруппа с сохраненным психическим статусом и многочисленными неокортикальными бляшками. Анналы неврологии. 1988;23(2):138–144. [PubMed] [Google Scholar]
14. Шофилд П.В., Логроскино Г., Эндрюс Х., Альберт С., Стерн Ю. Связь между окружностью головы и болезнью Альцгеймера в популяционном исследовании старения. Неврология. 1997; 49:30–37. [PubMed] [Google Scholar]
15. Стерн Ю. Что такое когнитивный резерв? Теория и исследовательское применение резервной концепции. Журнал Международного нейропсихологического общества. 2002; 8: 448–460. [PubMed] [Google Scholar]
2002; 8: 448–460. [PubMed] [Google Scholar]
16. Стерн Ю. Когнитивный резерв. Нейропсихология. 2009 г.;47:2015–2028. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Браун Дж., Купер-Кун С.М., Кемперман Г., ван Прааг Х., Винклер Дж., Гейдж Ф.Х. Обогащенная окружающая среда и физическая активность стимулируют нейрогенез гиппокампа, но не обонятельной луковицы. ЕВРОПЕЙСКИЙ ЖУРНАЛ НЕВРОНАУКИ. 2003;17:2042–2046. [PubMed] [Google Scholar]
18. van Praag H, Christie BR, Sejnowski TJ, Gage FH. Бег усиливает нейрогенез, обучение и долговременную потенциацию у мышей. Proc Natl Acad Sci U S A. 1999;96(23):13427–13431. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. van Praag H, Kemperman G, Gage FH. Бег увеличивает пролиферацию клеток и нейрогенез в зубчатой извилине взрослых мышей. Неврология природы. 1999; 2: 266–270. [PubMed] [Google Scholar]
20. van Praag H, Kempermann G, Gage FH. Нейронные последствия обогащения окружающей среды. Нат Рев Нейроски. 2000;1(3):191–198. [PubMed] [Google Scholar]
2000;1(3):191–198. [PubMed] [Google Scholar]
21. Valenzuela MJ, Sachdev P, Wen W, Chen X, Brodaty H. Умственная активность в течение жизни предсказывает снижение скорости атрофии гиппокампа. ПЛОС Один. 2008;3(7):e2598. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Landau SM, Marks SM, Mormino EC, Rabinovici GD, Oh H, O’Neil JP, et al. Ассоциация когнитивной активности на протяжении всей жизни и низкого уровня бета-амилоидных отложений. Арх Нейрол. 2012 [бесплатная статья PMC] [PubMed] [Google Scholar]
23. Stern Y, Gurland B, Tatemichi TK, Tang MX, Wilder D, Mayeux R. Влияние образования и профессии на заболеваемость болезнью Альцгеймера. Журнал Американской медицинской ассоциации. 1994; 271:1004–1010. [PubMed] [Академия Google]
24. Scarmeas N, Levy G, Tang MX, Manly J, Stern Y. Влияние досуга на заболеваемость болезнью Альцгеймера. Неврология. 2001;57(12):2236–2242. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Валенсуэла М.Дж. , Сачдев П. Мозговой резерв и деменция: систематический обзор. Психомед. 2005; 25:1–14. [PubMed] [Google Scholar]
, Сачдев П. Мозговой резерв и деменция: систематический обзор. Психомед. 2005; 25:1–14. [PubMed] [Google Scholar]
26. Stern Y, Tang MX, Denaro J, Mayeux R. Повышенный риск смертности у пациентов с болезнью Альцгеймера с более высоким уровнем образования и профессиональной подготовки. Анналы неврологии. 1995;37:590–595. [PubMed] [Google Scholar]
27. Stern Y, Albert S, Tang MX, Tsai WY. Скорость снижения памяти при БА связана с образованием и родом занятий: Когнитивный резерв? Неврология. 1999; 53: 1942–1957. [PubMed] [Google Scholar]
28. Скармиас Н., Альберт С.М., Мэнли Дж.Дж., Стерн Ю. Образование и темпы снижения когнитивных функций при болезни Альцгеймера. Журнал неврологии, нейрохирургии и психиатрии. 2006;77(3):308–316. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Helzner EP, Scarmeas N, Cosentino S, Portet F, Stern Y. Активность в свободное время и снижение когнитивных функций при заболевании болезнью Альцгеймера. Архив неврологии. 2007;64(12):1749–1754. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
30. Friedland RP, Brun A, Bundinger TF. Патологические и позитронно-эмиссионные томографические корреляции при болезни Альцгеймера. Ланцет. 1985: 1–228. [PubMed] [Google Scholar]
31. McGeer EG, Peppard RP, McGeer PL, et al. 18 Исследования позитронно-эмиссионной томографии с фтордезоксиглюкозой при подозрении на болезнь Альцгеймера, включая 13 последовательных сканирований. Канадский журнал неврологических наук. 1990;17:1–11. [PubMed] [Google Scholar]
32. Stern Y, Alexander GE, Prohovnik I, Mayeux R. Обратная связь между образованием и теменно-височным дефицитом перфузии при болезни Альцгеймера. Анналы неврологии. 1992; 32: 371–375. [PubMed] [Google Scholar]
33. Stern Y, Alexander GE, Prohovnik I, Stricks L, Link B, Lennon MC, et al. Взаимосвязь между занятием на протяжении всей жизни и пристеночным кровотоком: последствия для резерва против патологии болезни Альцгеймера. Неврология. 1995; 45: 55–60. [PubMed] [Академия Google]
34. Scarmeas N, Zarahn E, Anderson KE, Habeck CG, Hilton J, Flynn J, et al. Связь жизнедеятельности с мозговым кровотоком при болезни Альцгеймера — значение для гипотезы когнитивного резерва. Архив неврологии. 2003; 60: 359–365. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Scarmeas N, Zarahn E, Anderson KE, Habeck CG, Hilton J, Flynn J, et al. Связь жизнедеятельности с мозговым кровотоком при болезни Альцгеймера — значение для гипотезы когнитивного резерва. Архив неврологии. 2003; 60: 359–365. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Alexander GE, Furey ML, Grady CL, Pietrini P, Brady DR, Mentis MJ, et al. Связь преморбидной интеллектуальной функции с церебральным метаболизмом при болезни Альцгеймера: значение для гипотезы когнитивного резерва. Am J Психиатрия. 1997;154(2):165–172. [PubMed] [Google Scholar]
36. Perneczky R, Drzezga A, ehl-Schmid J, Schmid G, Wohlschlager A, Kars S, et al. Обучение в школе опосредует резерв мозга при болезни Альцгеймера: результаты фтор-дезокси-глюкозо-позитронно-эмиссионной томографии. J Neurol Нейрохирург Психиатрия. 2006;77(9):1060–1063. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Bennett DA, Wilson RS, Schneider JA, Evans DA, Mendes De Leon CF, Arnold SE, et al. Образование модифицирует отношение патологии БА к уровню когнитивной функции у пожилых людей. Неврология. 2003;60(12):1909–1915. [PubMed] [Google Scholar]
Неврология. 2003;60(12):1909–1915. [PubMed] [Google Scholar]
38. Stern Y, Habeck C, Moeller J, Scarmeas N, Anderson KE, Hilton HJ, et al. Сети мозга, связанные с когнитивным резервом у здоровых молодых и пожилых людей. Кора головного мозга. 2005;15(4):394–402. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Stern Y, Rakitin BC, Habeck C, Gazes Y, Steffener J, Kumar A, et al. Сложность задачи модулирует различия между молодыми и старыми в экспрессии сети. Мозг Res. 2012;1435:130–145. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Заран Э., Ракитин Б., Абела Д., Флинн Дж., Стерн Ю. Возрастные изменения в активации мозга во время задачи распознавания предметов с задержкой. Нейробиол Старение. 2007;28(5):784–798. [PubMed] [Google Scholar]
41. Steffener J, Brickman AM, Rakitin BC, Gazes Y, Stern Y. Влияние структуры на возрастные изменения функциональной активности рабочей памяти. Визуализация мозга и поведение. 2008 [Бесплатная статья PMC] [PubMed] [Google Scholar]
42. Штеффенер Дж., Рубен А., Ракитин Б.С., Стерн Ю. Поддержка производительности перед лицом возрастных нейронных изменений: проверка механистической роли когнитивного резерва. Поведение визуализации мозга. 2011 [Бесплатная статья PMC] [PubMed] [Google Scholar]
Штеффенер Дж., Рубен А., Ракитин Б.С., Стерн Ю. Поддержка производительности перед лицом возрастных нейронных изменений: проверка механистической роли когнитивного резерва. Поведение визуализации мозга. 2011 [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Стерн Ю., Заран Э., Хабек С., Хольцер Р., Ракитин Б.С., Кумар А. и соавт. Общая нейронная сеть для когнитивного резерва в вербальной и объектной рабочей памяти у молодых, но не старых. Кора головного мозга. 2008; 18: 959–967. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Garibotto V, Borroni B, Kalbe E, Herholz K, Salmon E, Holtoff V, et al. Образование и профессия как показатели резерва в преобразователях aMCI и AD: свидетельство FDG-PET. Неврология. 2008;71(17):1342–1349. [PubMed] [Академия Google]
45. Кемппайнен Н.М., Аалто С., Карраш М., Нагрен К., Сависто Н., Ойконен В. и соавт. Гипотеза когнитивного резерва: Питтсбургское соединение B и позитронно-эмиссионная томография с фтордезоксиглюкозой в отношении образования при легкой болезни Альцгеймера. Энн Нейрол. 2008;63(1):112–118. [PubMed] [Google Scholar]
Энн Нейрол. 2008;63(1):112–118. [PubMed] [Google Scholar]
46. Hall CB, Derby C, LeValley A, Katz MJ, Verghese J, Lipton RB. Образование задерживает ускоренное ухудшение результатов теста памяти у лиц, у которых развивается слабоумие. Неврология. 2007;69(17):1657–1664. [PubMed] [Академия Google]
47. Angevaren M, Aufdemkampe G, Verhaar H, Aleman A, Vanhees L. Физическая активность и улучшение физической формы для улучшения когнитивных функций у пожилых людей без известных когнитивных нарушений. Кокрановская система базы данных, ред. 2008; 2 CD005381. [PubMed] [Google Scholar]
48. Kramer AF, Hahn S, Cohen NJ, Banich MT, McAuley E, Harrison CR, et al. Старение, фитнес и нейрокогнитивные функции. Природа. 1999;400(6743):418–419. [PubMed] [Google Scholar]
49. Jobe JB, Smith DM, Ball K, Tennstedt SL, Marsiske M, Willis SL, et al. АКТИВНЫЙ: испытание когнитивной интервенции для развития самостоятельности у пожилых людей. Контрольные клинические испытания. 2001; 22(4):453–479. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Basak C, Boot WR, Voss MW, Kramer AF. Могут ли тренировки в стратегической видеоигре в реальном времени смягчить снижение когнитивных функций у пожилых людей? Психология и старение. 2008;23(4):765–777. [PMC free article] [PubMed] [Google Scholar]
51. Клингберг Т. Тренировка и пластичность рабочей памяти. Тенденции Cogn Sci. 2010;14(7):317–324. [PubMed] [Google Scholar]
52. Wykes T, Huddy V, Cellard C, McGurk SR, Czobor P. Метаанализ когнитивной реабилитации при шизофрении: методология и размеры эффекта. Am J Психиатрия. 2011;168(5):472–485. [PubMed] [Академия Google]
53. Королевское общество. Мозговые волны Модуль 2: Неврология: последствия для образования и обучения на протяжении всей жизни. 2011 [цит.; Доступно по адресу: http://royalsociety.org/uploadedFiles/Royal_Society/Policy_and_Influence/Module_2_Neuroscience_Education_Full_Report_Printer_Friendly.pdf.
54. Мане АДЭ. Игра «Космическая крепость». Acta Psychologica. 1989; 71: 17–22. [Google Scholar]
Acta Psychologica. 1989; 71: 17–22. [Google Scholar]
55. Fabiani M, Buckley J, Gratton G, Coles MGH, Donchin E. Обучение выполнению сложных задач. Acta Psychologica. 1989;71:259–299. [Google Scholar]
56. Гофер Д., Вейл М., Барекет Т. Перенос навыков из тренажера компьютерных игр в полет. Человеческие факторы. 1994;36(3):387–405. [Google Scholar]
57. Гофер Д., Вейл М., Сигал Д. Практика в условиях меняющихся приоритетов: подход к обучению сложным навыкам. Acta Psychologica. 1989; 71: 147–177. [Google Scholar]
58. Blumen HM, Gopher D, Steinerman JR, Stern Y. Тренировка когнитивного контроля у пожилых людей с помощью игры «Космическая крепость»: роль тренировочных инструкций и базовых двигательных способностей. Front Aging Neurosci. 2010;2:145. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Оррелл М., Саакян Б. Образование и деменция. БМЖ. 1995;310(6985):951–952. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Здоровое старение: когнитивный резерв и как его укрепить
Узнайте, почему ухудшение памяти может быть таким разным у людей одного возраста, даже у близкородственных людей.
Эндрю сопровождал своего отца Роберта в клинику памяти. Наше обследование показало, что у Роберта серьезное нейрокогнитивное расстройство, вероятно, болезнь Альцгеймера, а его память и исполнительные функции сильно нарушены. Эндрю не удивился, когда мы поставили этот диагноз, но он был расстроен из-за своего отца, а также спросил о своем собственном риске слабоумия. Он сказал: «Моему дяде Уолтеру 85 лет, и он до сих пор каждый день обходит больницу. Его пациенты говорят, что он все еще такой же острый, как и всегда. Но моему отцу всего 76, и он не помнит, как доехать до продуктового магазина! Как эти братья могли так по-разному состариться? Могу ли я как-то стареть, как мой дядя, а не как мой отец?»*
*Эндрю, Роберт и Уолтер похожи на многих людей, которых видели в Клинике расстройств памяти, но они являются составными персонажами, а не отдельными личностями для защиты частной жизни .
Почему ухудшение памяти так сильно различается у людей одного возраста, даже у близкородственных людей? Как мозг некоторых людей более успешно сопротивляется повреждениям, вызванным старением, травмами или деменцией, чем другие? Исследователи, изучающие визуализирующие исследования или результаты вскрытия, пытались понять, как один человек с легкими признаками повреждения головного мозга может быть серьезно инвалидизирован, в то время как у другого с обширными изменениями мозга наблюдаются лишь легкие когнитивные нарушения.
Даже у людей, перенесших черепно-мозговую травму или инсульт, когнитивные симптомы и восстановление когнитивных функций сильно различаются. Некоторые мозги просто кажутся более сильными и устойчивыми перед лицом старения или разрушительных событий. «Когнитивный резерв» — важная идея, проливающая свет на эту загадку.
Что такое когнитивный резерв?
Основная идея «когнитивного резерва» заключается в том, что некоторые мозги продолжают работать более успешно, чем другие, несмотря на одинаковую степень разрушения или дегенерации, и что это является следствием врожденных и приобретенных характеристик мозга. При рождении наш мозг уже отличается. Некоторые больше, некоторые меньше. Некоторые обладают более высокими специфическими или общими интеллектуальными возможностями. Но жизненный опыт, образование, профессия, питание и здоровье — все это оказывает решающее влияние на нашу жизнь.
Считается, что эти различия отражают качество внутренних связей мозга и здоровье. Здоровый, хорошо развитый, хорошо питающийся мозг и здоровое с медицинской точки зрения тело работают более эффективно. Он также противостоит последствиям травмы или инсульта или нарушениям, связанным с такими заболеваниями, как диабет, высокое кровяное давление или депрессия.
Здоровый, хорошо развитый, хорошо питающийся мозг и здоровое с медицинской точки зрения тело работают более эффективно. Он также противостоит последствиям травмы или инсульта или нарушениям, связанным с такими заболеваниями, как диабет, высокое кровяное давление или депрессия.
Положительные эффекты стимулирующей среды
В детстве когнитивно-стимулирующая среда способствует развитию большего объема мозга. Физические упражнения и когнитивная стимуляция увеличивают количество молекул, которые повышают способность мозга постоянно меняться на протяжении всей жизни человека. Это называется пластичностью мозга. Кроме того, эти молекулы также способствуют развитию структур, которые позволяют нервным клеткам передавать электрический или химический сигнал другим нервным клеткам, называемых синапсами.
Здоровый мозг в стимулирующей среде выращивает новые клетки и создает новые связи. Совокупный эффект интеллектуальных способностей, образования, опыта и профессии, по-видимому, оказывает важное влияние на то, как поврежденный мозг будет компенсировать и сохранять функционирование. Ухудшение памяти, исполнительных функций и языковых навыков, связанное с нормальным старением, происходит медленнее у людей с большей грамотностью.
Ухудшение памяти, исполнительных функций и языковых навыков, связанное с нормальным старением, происходит медленнее у людей с большей грамотностью.
В одном важном исследовании, например, люди с низким уровнем образования и низкой профессиональной успеваемостью почти в три раза чаще болели деменцией по сравнению с их более образованными и более успешными сверстниками. Было продемонстрировано, что даже в более позднем возрасте участие в когнитивно-стимулирующих досуговых мероприятиях повышает устойчивость к клинической деменции. Теория когнитивного резерва привела исследователей к открытию, что более высокотренированный мозг способен более эффективно использовать свои ресурсы и с большей готовностью задействовать дополнительные области мозга, когда это необходимо.
Парадокс
Это может показаться парадоксальным, но идея когнитивного резерва может также помочь нам понять, почему деменция у более высокообразованных людей может прогрессировать быстрее, как только она становится очевидной. Может существовать порог повреждения, который не может преодолеть даже самый высокоразвитый мозг. Хотя мозг с большим резервом дольше борется с последствиями деменции, истощение когнитивного резерва обычно приводит к более быстрому ухудшению состояния, поскольку основное разрушение уже было более обширным, чем можно было бы предположить по клиническим признакам. Даже среди здоровых пожилых людей ухудшение памяти развивается позже, но затем прогрессирует быстрее у лиц с высшим образованием.
Может существовать порог повреждения, который не может преодолеть даже самый высокоразвитый мозг. Хотя мозг с большим резервом дольше борется с последствиями деменции, истощение когнитивного резерва обычно приводит к более быстрому ухудшению состояния, поскольку основное разрушение уже было более обширным, чем можно было бы предположить по клиническим признакам. Даже среди здоровых пожилых людей ухудшение памяти развивается позже, но затем прогрессирует быстрее у лиц с высшим образованием.
Полезный совет по развитию и поддержанию здоровья мозга
Какой совет был дан Эндрю, когда он предвкушал свои последние годы? Одна из самых важных вещей в теории когнитивного резерва заключается в том, что она дает нам надежду на борьбу с последствиями старения мозга и дегенеративными расстройствами, хотя мы еще не смогли открыть лекарства, излечивающие деменцию.
Раннее образование, когнитивная стимуляция и физическая активность закладывают основу для дальнейшего здоровья мозга. Во взрослом возрасте продолжение обучения и активное участие в досуге могут усилить устойчивость к снижению когнитивных функций.
Во взрослом возрасте продолжение обучения и активное участие в досуге могут усилить устойчивость к снижению когнитивных функций.
Здоровье мозга дополнительно поддерживается физической активностью и хорошим уходом за собой, который включает достаточный сон и снижение стресса, хорошее питание и заботу о здоровье.
Индивидуальные генетические факторы, влияющие на риск деменции, пока не поддаются изменению, но на прогрессирование и проявления старения и болезней мозга сильно влияет то, как мы живем и как используем свой мозг. Эндрю, достаточно молодой, чтобы увеличить свою физическую и умственную деятельность, в состоянии улучшить долгосрочные перспективы своего когнитивного здоровья в последующие годы.
Когда мы узнали больше о семье Эндрю, стало ясно, что Уолтер и Роберт вели совершенно разные образы жизни. Уолтер учился в колледже и в аспирантуре и был успешным врачом-специалистом, которому нравились познавательно сложные хобби и обучение на протяжении всей жизни. Роберт закончил среднюю школу, но бросил колледж на первом курсе, чтобы поддержать своих стареющих родителей в их семейном бизнесе. Он был трудолюбивым, хорошим кормильцем для своей семьи и любимым человеком в своей общине. Но он обычно пренебрегал своим физическим здоровьем и досугом. С возрастом его образ жизни стал более сидячим, и он предпочитал использовать свое ограниченное свободное время для отдыха, а не для когнитивной стимуляции или физических упражнений. У него развились несколько хронических заболеваний, высокое кровяное давление и диабет, и его внимание к их лечению не было приоритетом. Возможно, это отчасти объясняло очень разный опыт старения братьев. Помимо различий, обусловленных генетикой, Уолтер, по-видимому, развил более высокий уровень когнитивного резерва. Уолтер тренировал свой разум и тело и заботился о своем здоровье более последовательно, чем Роберт. Эта разница в образе жизни может частично объяснить, почему разум Уолтера продолжал функционировать на высоком уровне, в то время как у Роберта он снижался.
Роберт закончил среднюю школу, но бросил колледж на первом курсе, чтобы поддержать своих стареющих родителей в их семейном бизнесе. Он был трудолюбивым, хорошим кормильцем для своей семьи и любимым человеком в своей общине. Но он обычно пренебрегал своим физическим здоровьем и досугом. С возрастом его образ жизни стал более сидячим, и он предпочитал использовать свое ограниченное свободное время для отдыха, а не для когнитивной стимуляции или физических упражнений. У него развились несколько хронических заболеваний, высокое кровяное давление и диабет, и его внимание к их лечению не было приоритетом. Возможно, это отчасти объясняло очень разный опыт старения братьев. Помимо различий, обусловленных генетикой, Уолтер, по-видимому, развил более высокий уровень когнитивного резерва. Уолтер тренировал свой разум и тело и заботился о своем здоровье более последовательно, чем Роберт. Эта разница в образе жизни может частично объяснить, почему разум Уолтера продолжал функционировать на высоком уровне, в то время как у Роберта он снижался.
- Шин М., Сон М., Ли Дж. и др. Влияние когнитивного резерва на риск когнитивных нарушений и восстановления после инсульта. Исследование КОСКО. Инсульт 2020;51:99-1-7.
- Штерн Ю. Когнитивный резерв. Нейропсихология 2009;47(10):2015-28.
- Stern Y, Gurland B, Tatemichi TK, et al. Влияние образования и профессии на заболеваемость болезнью Альцгеймера. ДЖАМА 1994 ;271:1004-1010
- Hall CB, Derby C, LeValley A и др. Образование задерживает ускоренное ухудшение результатов теста памяти у лиц, у которых развивается слабоумие. Неврология 2007;69:1657-64.
- Meng X, D’Arcy C. Образование и слабоумие в контексте гипотезы когнитивного резерва: систематический обзор с метаанализом и качественным анализом. PLoS ONE 2012;7(6):1-16.
- Сюй Х., Ян Р., Ци С. и др. Ассоциация показателя когнитивного резерва ПЖ с риском деменции при патологии головного мозга.

